
Les facteurs de risque de la dysfonction érectile sont multiples et intriqués (illustration).
VITAROS 300 µg crème (alprostadil) est nouveau médicament urologique indiqué chez les hommes à partir de 18 ans dans le traitement de la dysfonction érectile, définie par l'incapacité à atteindre ou à maintenir une érection suffisante du pénis pour permettre une performance sexuelle satisfaisante (Cf. Reco VIDAL Dysfonction érectile).
A propos l'alprostadil
Le principe actif de VITAROS 300 µg crème est l'alprostadil. Sa structure chimique est identique à celle la prostaglandine E1, qui agit par vasodilatation des vaisseaux sanguins du tissu érectile des corps caverneux et augmentation du débit des artères caverneuses, entraînant une rigidité pénienne.
L'alprostadil est actuellement disponible sur le marché français sous forme injectable pour une administration par voie intracaverneuse (CAVERJECT, EDEX) ou sous forme de bâton pour usage urétral (MUSE).
Place de VITAROS dans la stratégie thérapeutique
L'efficacité de VITAROS a été évaluée dans deux études pivot de phase III (MED 2000-004, 878 patients ; MED 2000-005, 854 patients) randomisées en double aveugle ont comparé VITAROS 100 µg, 200 µg et 300 µg au placebo pendant 12 semaines chez des patients atteints de dysfonction érectile d'étiologies diverses, incluant des dysfonctions érectiles secondaires à des maladies organiques ou en échec à un traitement par le sildénafil (Cf. Avis de la Commission de la transparence du 18 mars 2015).
Dans ces deux études, le score de fonction érectile du questionnaire IIEF (International Index of Erectile Function) a été statistiquement amélioré dans le groupe VITAROS comparativement au placebo.
Sachant qu'"[...] il est communément admis qu'une variation de + 3 à + 4 points par rapport aux scores initiaux est nécessaire pour être significative pour le patient [...]", la Commission de la transparence (CT) a estimé que "[...] la différence entre VITAROS et le placebo bien que statistiquement significative est faible [...]" :
- + 2,5 points et + 3,1 points dans les groupes alprostadil 200 µg et 300 µg versus - 0,5 point dans le groupe placebo dans l'étude MED 2000-004 ;
- + 2,4 points et + 1,7 point dans les groupes alprostadil 200 µg et 300 µg versus - 0,9 point dans le groupe placebo dans l'étude MED 2000-005.
Une augmentation du pourcentage de succès de la pénétration vaginale et de l'éjaculation a également été observée dans le groupe VITAROS comparativement au placebo. Selon l'avis de la CT, "L'effet de VITAROS apparaît également faible comparativement au placebo."
La CT a regretté "l'absence d'étude versus un traitement actif de la dysfonction érectile, en particulier les IPDE 5".
En termes d'effets indésirables, les événement les plus fréquemment rapportés ont été :
- une réaction urogénitale locale transitoire : sensation de chaleur ou de brûlure dans le pénis, douleur ou érythème pénien chez 36 à 43 % des patients,
- une réacion vaginale locale chez la partenaire, principalement à type de brûlures vaginales d'intensité légère à modérée dans 5 à 9 % des cas.
La CT a conclu que "VITAROS est une alternative aux spécialités à base d'alprostadil administrées par voie intra-caverneuse en cas d'échec ou de contre-indication aux inhibiteurs des phosphodiestérases de type 5 (IPDE 5)", qui restent le traitement pharmacologique de 1re intention des troubles de l'érection (VIAGRA, CIALIS, LEVITRA, SPEDRA).
VITAROS : délai et durée d'action
VITAROS se présente sous forme de récipient unidose à usage unique (Accudose) contenant 300 µg d'alprostodil.
L'érection apparaît dans un délai de 5 à 30 minutes suivant l'administration.
La demi-vie de l'alprostadil est courte et la durée de l'effet est d'environ 1 à 2 heures. Cependant, la durée effective est variable d'un patient à l'autre.
La fréquence d'utilisation ne doit pas dépasser 2 à 3 utilisations par semaine, à raison d'une seule fois par tranche de 24 heures.
L'utilisation de VITAROS est contre-indiquée dans les situations suivantes :
- troubles sous-jacents tels qu'une hypotension orthostatique, un infarctus du myocarde ou une syncope,
- hypersensibilité connue à l'alprostadil ou à l'un des autres composants de VITAROS,
- affections susceptibles de prédisposer le patient à un priapisme, telles qu'une anémie falciforme ou la présence du trait drépanocytaire, une hyperplaquettose, une polyglobulie, un myélome multiple ou une leucémie,
- chez les patients présentant une anomalie anatomique du pénis comme par exemple un hypospadias sévère ou d'une déformation anatomique du pénis, comme une courbure du pénis, et chez les patients présentant une urétrite ou une balanite (inflammation/infection du gland du pénis),
- patient présentant un risque de thrombose veineuse ou présentant un syndrome d'hyperviscosité et donc exposé à un risque accru de priapisme (rigidité pénienne se prolongeant 4 heures ou plus),
- patients pour lesquels une activité sexuelle est déconseillée, comme par exemple en cas d'instabilité cardiovasculaire ou cérébrovasculaire,
- lors de rapports sexuels avec une femme en âge de procréer, sauf si le couple utilise un préservatif.
En pratique : le patient doit être formé à la technique d'auto-administration
Le récipient unidose Accudose se compose d'un piston, d'un cylindre formant le corps du dispositif et d'un capuchon de protection. Il est fourni dans un sachet protecteur.
Préalablement à toute auto-administration, chaque patient doit être formé à la technique d'auto-administration de VITAROS par un professionnel de santé (Cf. figure 1 et Notice du médicament) et notamment :
- VITAROS doit être manipulé avec des mains propres.
- L'embout du récipient unidose ne doit pas être introduit dans le méat urétral.
- La totalité de la crème contenue dans le récipient doit être utilisée.
- Elle doit être appliquée à l'extrémité du pénis au niveau du méat urétral.
Figure 1 : Mode d'administration de VITAROS (extrait du résumé des caractéristiques du produit)
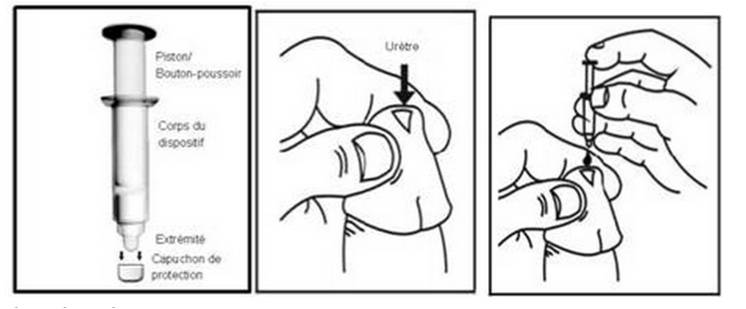
- Après administration de la crème, le pénis doit être tenu à la verticale pendant environ 30 secondes afin de permettre une bonne pénétration du produit.
- Si une partie de la dose reste sur le bord du méat urétral, il est possible de faire pénétrer cet excès de crème dans la peau entourant le site d'application en le massant délicatement du bout du doigt.
- Un deuxième récipient unidose AccuDose ne doit pas être utilisé pour compenser la crème n'ayant pas pénétré dans le méat.
Conseils au patient
VITAROS est à conserver au réfrigérateur, entre 2 °C et 8 °C.
Toutefois, les sachets non entamés peuvent être conservés par le patient en dehors du réfrigérateur pendant 3 jours au maximum avant utilisation, à une température ne dépassant pas 25 °C.
Il est important de rappeler aux patients que VITAROS n'offre aucune protection contre la transmission des maladies sexuellement transmissibles (MST), et ne présente pas de propriétés contraceptives.
Les partenaires d'utilisateurs de VITAROS peuvent présenter des événements indésirables, du type irritation vaginale essentiellement.
Les professionnels de santé doivent encourager leurs patients à informer leurs partenaires sexuels qu'ils utilisent VITAROS, et à utiliser un préservatif, notamment pour les femmes en âge de procréer. A noter que seuls des préservatifs à base de latex ont fait l'objet d'études lors de l'utilisation du produit.
En cas de priapisme (érection prolongée pendant plus de 4 heures), une consultation médicale immédiate est nécessaire.
Un remboursement demandé par le laboratoire pour certaines catégories de patients
Le laboratoire a déposé auprès de la Haute Autorité de santé (HAS) une demande de remboursement pour VITAROS dans le traitement de seconde intention des dysfonctions érectiles d'origine organique :
- paraplégie et tétraplégie quelle qu'en soit l'origine ;
- traumatisme du bassin compliqué de troubles urinaires ;
- séquelles de la chirurgie (anévrisme de l'aorte ; prostatectomie radicale, cystectomie totale et exérèse colorectale) ou de la radiothérapie abdominopelvienne ;
- séquelles du priapisme ;
- neuropathie diabétique avérée ;
- sclérose en plaques.
EDIT du 8 juillet 2015 : VITAROS est remboursable et agréé aux collectivités à compter du 12 juillet 2015 (arrêté du 3 juillet 2015 publié au Journal officiel du 8 juillet 2015), dans le traitement des dysfonctions érectiles d'origine organique :
- paraplégie et tétraplégie quelle qu'en soit l'origine ;
- traumatisme du bassin compliqué de troubles urinaires ;
- séquelles de la chirurgie (anévrisme de l'aorte ; prostatectomie radicale, cystectomie totale et exérèse colorectale) ou de la radiothérapie abdominopelvienne ;
- séquelles du priapisme ;
- neuropathie diabétique avérée ;
- sclérose en plaques.
La prescription doit être réalisée sur une ordonnance de médicament d'exception, en conformité avec la fiche d'information thérapeutique. /EDIT
Le prix public TTC de VITAROS (boîte de 4 unidoses) devrait être compris entre 40 et 45 € selon les informations recueillies par VIDAL auprès du laboratoire.
EDIT du 8 juillet 2015 : Le prix public TTC est de 40,18 euros. /EDIT
Les IPDE 5, médicaments de 1re intention dans les troubles de l'érection, ne sont quant à eux pas remboursables actuellement.
Parmi les spécialités à base d'alprostadil :
- EDEX et CAVERJECT, administrés par voie intracaverneuse, sont remboursables à 30 % sur le même périmètre d'indications que celui sollicité pour le remboursement de VITAROS,
- MUSE, dont la voie d'administration est intra-urétrale, n'est pas remboursable.
Identité administrative
- Liste I
- Boîte de 4 récipients unidoses de 100 mg, CIP 3400927543876
- Non remboursable et non agréé aux collectivités (demande en cours)
- EDIT du 8 juillet 2015 : remboursable et agréé aux collectivités à compter du 12 juillet 2015, dans les conditions précisées par la FIT publiée au Journal officiel du 8 juillet 2015 (médicament d'exception). Taux de remboursement 15 %, prix public TTC = 40,18 euros /EDIT
- Laboratoire Majorelle
Pour aller plus loin
Avis de la Commission de la Transparence (HAS, 18 mars 2015)
Questionnaire IIEF (International Index of Erectile Function)
Fiche d'information thérapeutique (Journal officiel du 8 juillet 2015)
Sources
Commentaires
Ajouter un commentaire
En cliquant sur "Ajouter un commentaire", vous confirmez être âgé(e) d'au moins 16 ans et avoir lu et accepté les règles et conditions d'utilisation de l'espace participatif "Commentaires" .
Nous vous invitons à signaler tout effet indésirable susceptible d'être dû à un médicament en le déclarant en ligne.
Les plus récents

Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 7 minutes
7 minutes 7 commentaires
7 commentaires 


Ayant subi une prostatectomie radicale, j'utilise vitaros depuis 2 mois.les débuts étaient décourageants mais le produit a agi de plus en plus. Au bout de 8 applications, le résultat est là, une belle érection comme auparavant. Ça ne fonctionne pas toujours à 100 %(excitation moindre, dérangé durant l'acte par un coup de téléphone...) mais dans mon cas cela fonctionne (on peut coupler avec un vaccum)