Rotavirus en microscopie électronique (photo @ FP Williams, U.S. EPA, sur Wikimedia).
Davantage d'effets indésirables graves, 2 décès signalés
Dans un point d'information publié sur son site le 31 mars 2015, l'Agence nationale de sécurité du médicament et des produits de santé (ANSM) communique de récentes données de pharmacovigilance, notifiées en France depuis le début de la commercialisation des deux vaccins contre les rotavirus, ROTARIX (mai 2006) et ROTATEQ (janvier 2007) et jusqu'au 31 octobre 2014.
Il en ressort que, sur plus d'un million de doses distribuées :
- 508 notifications d'effets indésirables médicalement confirmées, dont 201 graves, ont été recueillies et analysées,
- parmi les observations graves, 47 cas d'invaginations intestinales aiguës, survenues dans le mois suivant la vaccination, ont été rapportés, dont "quelques-uns d'évolution fatale".
Plus précisément, selon les données issues de la réunion du Comité technique de Pharmacovigilance du 10 février 2015, la répartition des effets indésirables de ces vaccins en fonction du type et de la gravité est la suivante (extrait du compte rendu) :
- pour ROTARIX :
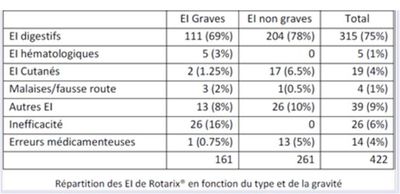
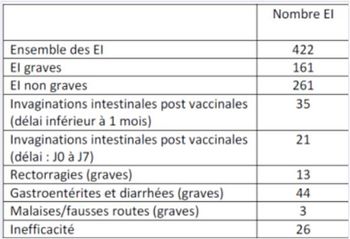
Parmi les 21 cas d'IIA survenus dans les 7 jours suivant la vaccination par ROTARIX, 3 cas ont été particulièrement graves, dont 2 hospitalisations (5,7 %) en réanimation et 1 décès (2,8 %).
- pour ROTATEQ :
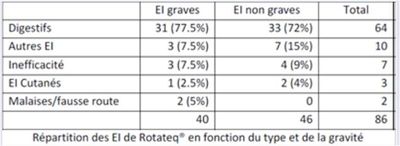
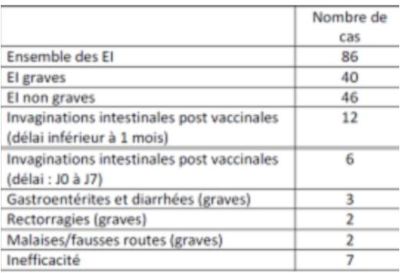
Parmi les 6 cas d'IIA survenus dans les 7 jours suivant la vaccination par ROTATEQ, 1 cas est survenu après la 3e dose et a évolué vers le décès (8,3 %).
Le bilan international des données de pharmacovigilance rapportées depuis la mise sur le marché des vaccins contre les infections à rotavirus fait état dans le monde :
- pour ROTARIX :
- d'un total de 23 450 effets indésirables (EI), dont 10 361 EI graves (44%) de juillet 2004 au 31 mai 2013,
- de 650 cas d'IIA (toutes graves), 48 cas de cyanose, 30 cas d'apnée, 64 cas d'hypersensibilité et 13 cas de maladie de Kawasaki (dont 12 graves).
- pour ROTATEQ :
- d'un total de 21 174 EI, dont 7 582 EI graves (36%) depuis novembre 2005 jusqu'au 27 novembre 2013,
- de 944 cas d'IIA (dont 905 graves), 88 cas d'apnée et 62 cas de maladie de Kawasaki (dont 61 graves).
En pratique : sensibiliser les familles
Compte tenu de ces données préoccupantes, les membres du Comité technique de pharmacovigilance (CTPV) se sont interrogés sur le bien-fondé de recommander la généralisation de cette vaccination en France et ont demandé que ce rapport soit transmis rapidement à la Haute Autorité de Santé et à la Direction Générale de la Santé.
Le CTPV a par ailleurs préconisé que des informations soient transmises aux professionnels de santé et aux familles sur la gravité de ces effets indésirables.
Dans ce contexte, l'ANSM a publié une mise au point où elle invite les professionnels de santé à sensibiliser les familles sur les signes d'invagination intestinale aiguë, survenant dans le mois suivant la vaccination, devant les amener à consulter sans délai leur médecin :
- douleurs abdominales,
- pleurs répétés et inhabituels de l'enfant,
- vomissement,
- présence de sang dans les selles,
- ballonnements abdominaux
- et/ou fièvre élevée.
Le HCSP prévoit de réexaminer ses recommandations de 2014
En mai 2014, le Haut Conseil de la santé publique (HCSP) publiait un avis relatif à la vaccination des nourrissons vis-à-vis des gastroentérites à rotavirus, où il recommandait notamment :
- la vaccination contre les rotavirus des nourrissons âgés de moins de 6 mois selon un schéma vaccinal à 2 doses (2 et 3 mois de vie) pour le vaccin monovalent (ROTARIX) et à 3 doses (2, 3 et 4 mois de vie) pour le vaccin pentavalent (ROTATEQ), en précisant que cette stratégie ne devrait être mise en place que si les prix des vaccins conduisent à des ratios coût/efficacité acceptables ;
- la poursuite du suivi renforcé de pharmacovigilance, initié en janvier 2012, relatif à la notification des invaginations intestinales aiguës ;
- que l'information sur le risque d'invagination intestinale aiguë soit systématiquement délivrée par les professionnels de santé aux parents des enfants vaccinés.
Le HCSP avait alors pris en considération les données de surveillance du Réseau sentinelle, du Programme de médicalisation des systèmes d'information (PMSI) et du Cépi-DC selon lesquelles les gastroentérites aiguës à rotavirus (GEA-RV) donnent lieu chaque année, chez les enfants âgés de moins de 3 ans, à environ :
- 155 000 consultations en médecine générale,
- 30 000 recours aux urgences hospitalières (période 2009-2012),
- 14 000 hospitalisations,
- un nombre de décès estimé entre 7,6 à 17,3 par an.
Les dernières données de pharmacovigilance publiées par le CTPV conduisent le HCSP a prévoir de réexaminer dans les prochains jours ses recommandations relatives à la vaccination des nourrissons contre les infections à rotavirus.
Pour aller plus loin
Vaccins contre les rotavirus (RotaTeq et Rotarix) et rappel sur la prise en charge de l'invagination intestinale aiguë du nourrisson - Point d'Information (ANSM, 31 mars2015)
Réunion du Comité technique de Pharmacovigilance – CT012015023 - Séance du mardi 10 février 2015 (ANSM, 31 mars 2015)
Avis du HCSP du 29 novembre 2013 relatif à la vaccination des nourrissons vis-à-vis des gastroentérites à rotavirus (mis en ligne le 14 février 2014)
Calendrier des vaccinations et recommandations vaccinales 2015 sur le site du Ministère des Affaires sociales, de la Santé et des Droits des femmes
Sur VIDAL.fr
Vaccination des nourrissons contre les rotavirus : recommandée par le HCSP (18 février 2014)
Pour aller plus loin
Consultez les monographies VIDAL
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes 8 commentaires
8 commentaires 


Commentaires
Cliquez ici pour revenir à l'accueil.