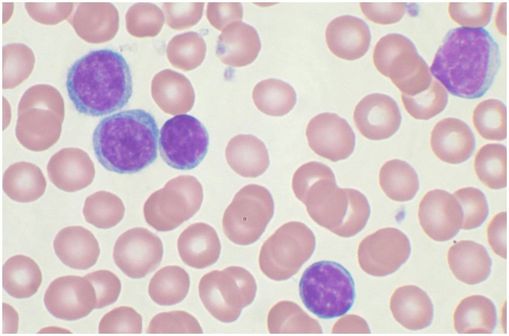
Lymphocytes B (cytoplasme bleu et noyau violet) lors d'une leucémie lymphoïde chronique observés sur sang périphérique (cliché @ Mary Ann Thompson sur Wikimedia).
IMBRUVICA 140 mg gélule (ibrutinib) est un nouveau médicament anticancéreux disponible à l'hôpital, en relais d'autorisation temporaire d'utilisation (ATU) de cohorte.
Ce médicament orphelin est indiqué :
- dans le traitement des patients adultes atteints d'un lymphome à cellules du manteau (LCM) en rechute ou réfractaire ;
- dans le traitement des patients adultes atteints d'une leucémie lymphoïde chronique (LLC) ayant reçu au moins un traitement antérieur, ou en première ligne en cas de délétion 17p ou de mutation TP53 chez les patients pour lesquels une immuno-chimiothérapie est inadaptée.
A propos de l'ibrutinib
L'ibrutinib est une petite molécule, puissante, inhibitrice de la tyrosine kinase de Bruton (BTK).
Les études précliniques ont montré que l'ibrutinib inhibe efficacement la prolifération et la survie in vivo des cellules B malignes ainsi que la migration cellulaire et l'adhésion au substrat in vitro.
Deux indications, deux posologies
La posologie recommandée d'IMBRUVICA est différente selon l'indication :
- pour le traitement du LCM, la posologie est de 560 mg (soit 4 gélules) 1 fois par jour ;
- pour le traitement de la LLC, la posologie est de 420 mg (soit 3 gélules) 1 fois par jour.
- le traitement doit être instauré et surveillé par un médecin expérimenté dans l'utilisation de médicaments anticancéreux ;
- le traitement doit être poursuivi jusqu'à progression de la maladie ou intolérance du patient.
- d'utilisation concomitante d'inhibiteurs modérés et puissants du CYP3A4, en raison du risque d'augmentation de l'exposition à l'ibrutinib. La posologie d'IMBRUVICA doit être réduite ou le traitement doit être interrompu (voir monographie VIDAL d'IMBRUVICA) ;
- en cas d'effets indésirables.
Conseils aux patients
IMBRUVICA doit être administré par voie orale 1 fois par jour avec un verre d'eau, approximativement au même moment chaque jour. Les gélules doivent être avalées entières avec de l'eau, sans être ouvertes, cassées, ni mâchées.
IMBRUVICA ne doit pas être pris avec du jus de pamplemousse ou des oranges de Séville (oranges amères). Ces produits contiennent des inhibiteurs du CYP3A4, leur administration concomitante augmente l'exposition de l'ibrutinib.
L'utilisation de préparations contenant du millepertuis est contre-indiquée chez les patients traités par IMBRUVICA. L'administration concomitante de ces préparations peut réduire l'efficacité d'IMBRUVICA.
Les femmes en âge de procréer doivent utiliser une méthode de contraception hautement efficace lors du traitement par IMBRUVICA et jusqu'à 3 mois après la fin du traitement. Les femmes utilisant une méthode de contraception hormonale doivent ajouter une méthode de contraception mécanique.
Identité administrative
- Liste I
- Prescription hospitalière réservée aux spécialistes en hématologie ou aux médecins compétents en maladie du sang
- Surveillance particulière pendant le traitement
- Boîte de 90 gélules, CIP 3400927949845
- Boîte de 120 gélules, CIP 3400927949906
- Prise en charge par les collectivités et rétrocession avec prise en charge à 100 % par l'assurance maladie en relais de l'ATU de cohorte
- Non remboursable, demande d'admission à l'étude
- Laboratoire Janssen-Cilag
Pour aller plus loin
Se reporter à la monographie VIDAL d'IMBRUVICA (mise à jour du 28 novembre 2014)
Résumé à l'intention du public (EMA, 25 novembre 2014)

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.