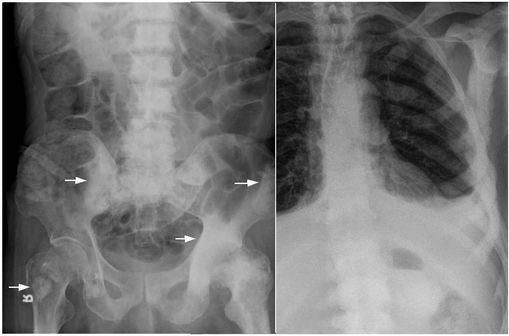
Métastases osseuses chez des patients atteints d'un cancer de la prostate (clichés @ Wikimedia).
Le médicament XOFIGO 1000 kBq/mL solution injectable (dichlorure de radium 223) fait actuellement l'objet d'une rupture de stock pour une durée indéterminée.
Selon les informations communiquées par le laboratoire Bayer, cette situation mondiale est consécutive à la détection, lors de contrôles de routine en cours de production, d'une non-conformité de lots récemment fabriqués et non encore distribués.
Des interruptions de traitement à prévoir
"Cette rupture temporaire d'approvisionnement peut avoir un impact sur la prise en charge des patients", indique le laboratoire dans un courrier adressé aux professionnels de santé. Il est donc recommandé de ne pas initier de nouveaux traitements par XOFIGO.
En outre, pour les patients recevant déjà XOFIGO, des interruptions de traitement sont à prévoir. Dans ce cas, les professionnels de santé concernés doivent envisager la nécessité de proposer un autre traitement, après évaluation clinique de chaque patient (voire la Reco VIDAL "Cancer de la prostate).
Les risques et les bénéfices liés à un changement de traitement doivent également être considérés.
Quel impact lors d'un retard d'administration ?
Afin de fournir des éléments relatifs au retard d'administration de XOFIGO chez des patients en cours de traitement, le laboratoire s'est appuyé sur les données de l'étude de phase III ALSYMPCA.
Ces données suggèrent qu'un retard d'administration n'excédant pas 4 semaines n'a pas de réel impact sur la survie globale. "Cependant, ces données doivent être interprétées avec prudence car elles sont basées sur des analyses de sous-groupes qui n'étaient pas prévues dans le protocole", précise le laboratoire.
Il n'existe pas de données sur l'impact possible d'un retard de traitement plus important.
Pour mémoire
XOFIGO solution isotonique injectable (dichlorure de radium 223) est un médicament réservé à l'usage hospitalier.
Il est indiqué chez l'adulte dans le traitement du cancer de la prostate résistant à la castration, avec métastases osseuses symptomatiques et sans métastases viscérales connues.
Pour aller plus loin
XOFIGO 1000 kBq/mL solution injectable (radium (223Ra)) - Rupture de stock (ANSM, 27 octobre 2014)
Lettre du laboratoire Bayer aux médecins nucléaires, oncologues, urologues, radiothérapeutes, radiopharmaciens et pharmaciens des centres de médecine nucléaire, centres investigateurs (sur le site de l'ANSM, octobre 2014)
Sur VIDAL.fr
Consulter la monographie VIDAL de XOFIGO (mise à jour du 16 octobre 2014)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 2 minutes
2 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.