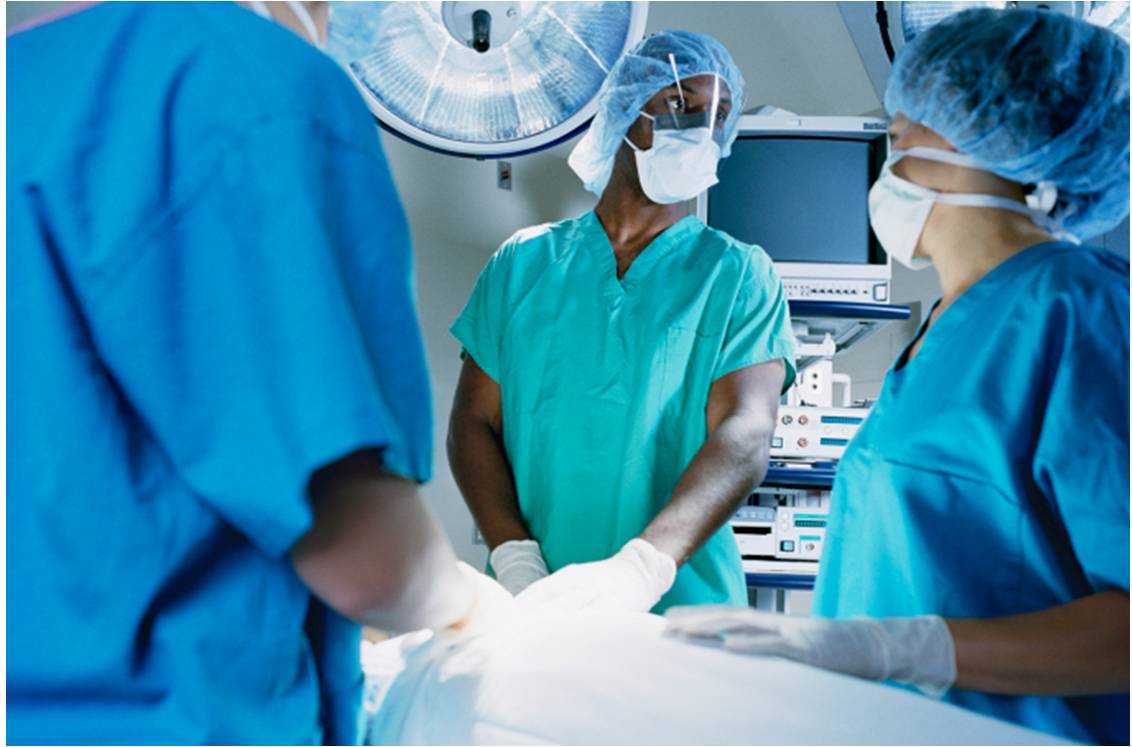
DANTRIUM IV est indiqué dans le traitement de l'hyperthermie maligne per-anesthésique, en association avec les mesures générales de prise en charge.
En mai dernier, le laboratoire Merck Serono avait signalé des problèmes de production concernant DANTRIUM intraveineux (IV) lyophilisat pour préparation injectable (dantrolène sodique). Afin d'éviter une rupture de stock, il avait décidé de prolonger de 6 mois la date de péremption des lots disponibles sur le marché (Cf. Article du 20 mai 2014).
En effet, en raison de ce problème de fabrication, certains flacons de DANTRIUM IV pouvaient contenir des cristaux non dissous de dantrolène sodique après reconstitution.
Ce problème n'est à ce jour pas résolu. Aussi, pour assurer la continuité de l'approvisionnement en DANTRIUM IV jusqu'à résolution du problème de fabrication, le laboratoire Merck Serono, en accord avec l'ANSM (Agence nationale de sécurité du médicament et des produits de santé), met à disposition sur le marché français des étuis de DANTRIUM IV lyophilisat pour préparation injectable fournis avec une aiguille filtre émoussée (aiguille BD Blunt Fill Needle-Filter de 5 microns 18 G et 40 mm).
Cette modification de conditionnement permet de réduire le risque d'administration de cristaux de dantrolène non dissous aux patients.
Une filtration nécessaire à partir du lot 154159
Toutes les boîtes de DANTRIUM IV libérées à partir du 1er août 2014 sont fournies avec l'aiguille filtre.
Cependant, les lots actuellement sur le marché ne sont pas concernés et ne nécessitent pas de filtration.
Ces mesures de filtration sont applicables à partir du lot 154159 (péremption 03/2017), mis en distribution à compter de début septembre. Ainsi, la solution de dantrolène sodique reconstituée à partir des flacons mis en distribution à compter de cette date doit être aspirée à l'aide de cette aiguille filtre pour réduire le risque d'administration de cristaux non dissous.
En pratique
Le laboratoire a adressé aux professionnels de santé un courrier dans lequel sont décrites les instructions de filtration.
La filtration ne modifie pas la quantité de dantrolène en solution et aucune réduction de l'efficacité de la solution n'est attendue.
Risque de réactions au site d'injection
Un risque de réactions au site d'injection est associé au dantrolène sodique, incluant érythème, éruption cutanée, oedème, douleur localisée, thrombophlébite et nécrose tissulaire.
Ce risque peut être accru par les particules pouvant être contenue dans les flacons des lots mis en distribution à compter de début septembre (à partir du lot 154159).
Pour mémoire
DANTRIUM IV est indiqué dans le traitement de l'hyperthermie maligne per-anesthésique, en association avec les mesures générales de prise en charge.
Pour aller plus loin
DANTRIUM intraveineux, lyophilisat pour préparation injectable: modification du conditionnement pour réduire le risque lors de l'administration (ANSM, 27 août 2014)
Lettre du laboratoire Merck Serono aux professionnels de santé (sur le site de l'ANSM, août 2014)
DANTRIUM intraveineux, lyophilisat pour préparation injectable - Remise à disposition (ANSM, 27 août 2014)
Sur www.vidal.fr
DANTRIUM INTRAVEINEUX (dantrolène) : report de la date de péremption pour 6 lots (20 mai 2014)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 2 minutes
2 minutes Ajouter un commentaire
Ajouter un commentaire





Commentaires
Cliquez ici pour revenir à l'accueil.