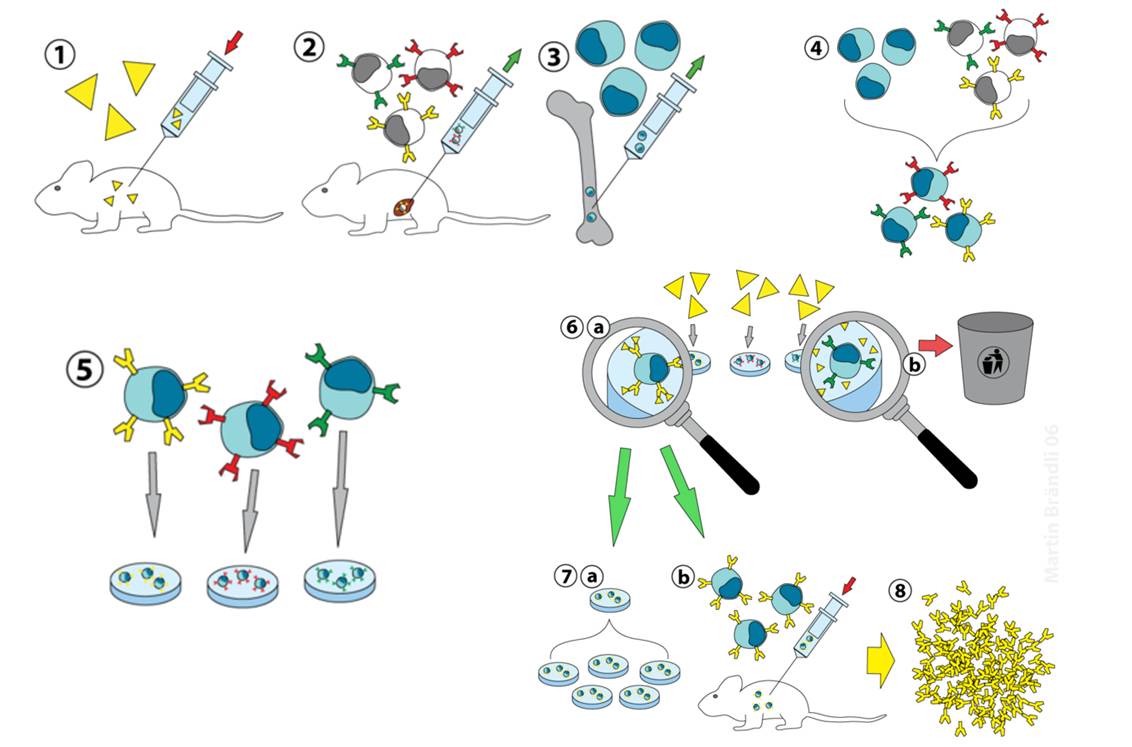
Représentation schématique du processus d'obtention d'anticorps monoclonaux (@ Martin Brändli, Wikimedia).
Depuis le 4 avril 2014, la spécialité ROACTEMRA 20 mg/ml solution à diluer pour perfusion (tocilizumab) fait l'objet d'une recommandation temporaire d'utilisation (RTU) concernant une maladie rare, la maladie de Castleman.
Selon cette RTU, ROACTEMRA peut être utilisé dans le traitement de la maladie de Castleman inflammatoire (à C-reactic protein [CRP)] élevée), non associée l'herpès virus humain 8 (HHV8).
Selon un arrêté du 21 août 2014, publié au Journal officiel du 26 août 2014, ROACTEMRA peut désormais être pris en charge dans cette indication pour une durée de trois ans, si son utilisation est indispensable à l'amélioration de l'état de santé du patient ou pour éviter sa dégradation.
ROACTEMRA et la maladie de Castleman
La maladie de Castleman est un syndrome lymphoprolifératif rare dont le traitement des formes disséminées n'est pas standardisé.
Selon plusieurs études, ROACTEMRA offre une alternative à la chimiothérapie dans les formes non plasmocytaires, non associées au virus HHV8, inflammatoires (CRP élevée) et symptomatiques de la maladie de Castleman.
Au cours de plusieurs essais cliniques, ROACTEMRA a montré une efficacité sur les symptômes de la maladie de Castleman, notamment une amélioration de la fatigue et de la fièvre, une diminution des adénopathies, une augmentation du poids, une normalisation de la CRP, une augmentation de l'hémoglobine, du fer sérique et du nombre de globules rouges.
La prise en charge en pratique
La prise en charge est réalisée dans les mêmes conditions que celles qui s'appliquent aux indications de l'autorisation de mise sur le marché (AMM).
Trois mois après le début de l'application du protocole de soins, le médecin-conseil et le médecin traitant doivent évaluer conjointement l'opportunité médicale du maintien de la prescription de ROACTEMRA.
Pour mémoire
La spécialité ROACTEMRA a reçu une AMM européenne (autorisation de mise sur le marché) dans les indications suivantes :
- En association au méthotrexate (MTX), le traitement de la polyarthrite rhumatoïde (PR) active, modérée à sévère, chez les patients adultes qui ont présenté soit une réponse inadéquate, soit une intolérance à un précédent traitement par un ou plusieurs traitements de fond (DMARDs) ou par un ou plusieurs antagonistes du facteur de nécrose tumorale (anti-TNF). Chez ces patients, ROACTEMRA peut être utilisé en monothérapie en cas d'intolérance au MTX, ou lorsque la poursuite du traitement par MTX est inadaptée. Il a été montré que ROACTEMRA, en association avec le méthotrexate, réduit le taux de progression des dommages structuraux articulaires mesurés par radiographie et améliore les capacités fonctionnelles.
- Le traitement de l'arthrite juvénile idiopathique systémique (AJIs) active chez les patients âgés de 2 ans et plus, qui ont présenté une réponse inadéquate à un précédent traitement par AINS et corticoïdes systémiques. ROACTEMRA peut être utilisé en monothérapie (en cas d'intolérance au MTX ou lorsque le traitement par MTX est inadapté) ou en association au MTX.
- En association au méthotrexate (MTX), le traitement de l'arthrite juvénile idiopathique polyarticulaire (AJIp ; facteur rhumatoïde positif ou négatif et oligoarthrite étendue) chez les patients âgés de 2 ans et plus, qui ont présenté une réponse inadéquate à un précédent traitement par MTX. ROACTEMRA peut être utilisé en monothérapie en cas d'intolérance au MTX, ou lorsque la poursuite du traitement par MTX est inadaptée.
ROACTEMRA est réservé à l'usage hospitalier.
La prescription de ROACTEMRA est réservée aux spécialistes en rhumatologie ou en médecine interne.
Pour aller plus loin
Arrêté du 21 août 2014, publié au Journal officiel du 26 août 2014
Fiche RTU ROACTEMRA (ANSM, 7 avril 2014)
L'ANSM publie une recommandation temporaire d'utilisation (RTU) concernant la spécialité Roactemra (tocilizumab) dans la maladie de Castleman - Point d'information (ANSM, 3 avril 2014)
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire.jpg)
.jpg)
.jpg)
.jpg)




Commentaires
Cliquez ici pour revenir à l'accueil.