
Vision avec une dégénérescence maculaire (@ Wikimedia).
LUCENTIS 10 mg/ml solution injectable (ranibizumab) est désormais disponible en seringue préremplie.
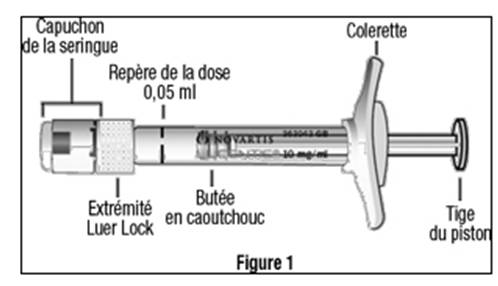
Cette nouvelle présentation s'ajoute à celle déjà commercialisée, LUCENTIS 10 mg/ml solution injectable en flacon de 0,23 ml.
La seringue préremplie en pratique
Une seringue préremplie de LUCENTIS 10 mg/ml solution injectable contient 0,165 ml de solution stérile, soit 1,65 mg de ranibizumab.
Le volume extractible d'une seringue préremplie est de 0,1 ml : il correspond à une dose de produit supérieure à la dose recommandée de 0,5 mg.
En conséquence, le volume extractible ne doit pas être utilisé en totalité.
Le volume excédentaire doit être éliminé avant l'injection, afin de ne délivrer qu'une dose unique de 0,05 ml contenant 0,5 mg de ranibizumab, correspondant à la posologie recommandée de LUCENTIS.
Pour éliminer les bulles d'air en même temps que l'excédent de solution, le piston doit être poussé lentement jusqu'à aligner le plateau situé en dessous de la partie bombée de la butée en caoutchouc avec le trait de dose noir de la seringue (équivalent à 0,05 ml, soit 0,5 mg de ranibizumab).
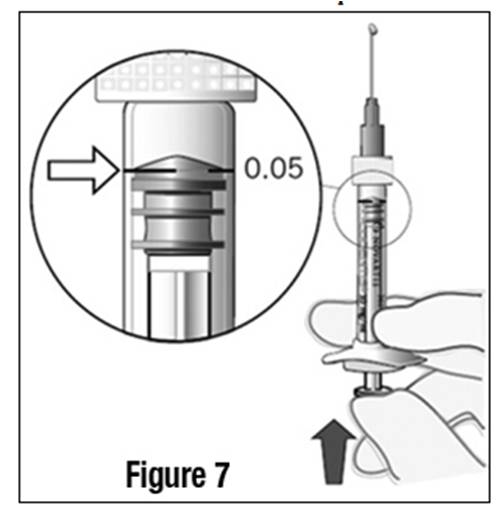
Chaque seringue préremplie ne doit être utilisée que pour traiter un seul oeil.
Pour l'injection intravitréenne, une aiguille stérile pour injection de 30 G x ½" doit être utilisée.
Les modalités de manipulation et d'élimination sont détaillées dans la monographie VIDAL de LUCENTIS.
Identité administrative
- Liste I
- Prescription réservée aux spécialistes en ophtalmologie
- Médicament d'exception : prescription en conformité avec la fiche d'information thérapeutique
- Boîte unitaire contenant 1 seringue préremplie, CIP 3400927671197
- Prix public TTC = 827,21 euros
- Remboursable à 100 % chez l'adulte dans :
- le traitement de la dégénérescence maculaire liée à l'âge (DMLA) exsudative avec une néovascularisation choroïdienne rétrofovéolaire ;
- le traitement de la baisse visuelle due à l'oedème maculaire diabétique (OMD) chez les patients ayant une baisse d'acuité visuelle inférieure ou égale à 5/10 consécutive à un oedème maculaire diabétique en cas de forme diffuse ou de fuites proches du centre de la macula et chez lesquels la prise en charge du diabète a été optimisée ;
- le traitement de la baisse visuelle due à l'oedème maculaire secondaire à une occlusion de branche veineuse rétinienne (OBVR) ou de la veine centrale de la rétine (OVCR) ;
- le traitement de la baisse visuelle due à une néovascularisation choroïdienne (NVC) secondaire à une myopie forte (MF).
- Agrément aux collectivités
- Laboratoire Novartis Pharma
Pour aller plus loin
Fiche d'information thérapeutique (Arrêté du 30 avril 2014 paru au Journal officiel du 7 mai 2014)
Avis de la Commission de la transparence du 5 février 2014 (HAS)
Sur www.vidal.fr
LUCENTIS (ranibizumab) : nouvelle indication remboursable dans le contexte d'une myopie forte (12 mai 2014)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 2 minutes
2 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.