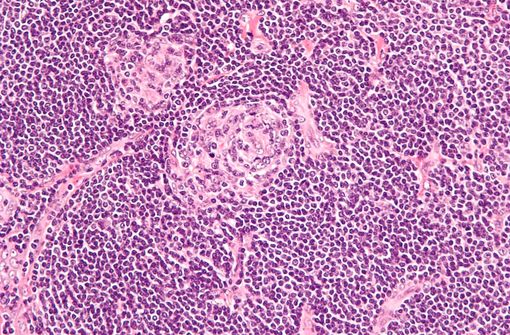
La maladie de Castleman est un trouble lymphoprolifératif rare qui peut être localisée à un seul ganglion lymphatique (monocentrique) ou être systémique (multicentrique). Photo © WIKIPEDIA
Quelques semaines après celle accordée au baclofène dans le traitement de la dépendance à l'alcool, une nouvelle RTU (recommandation temporaire d'utilisation) vient d'être publiée par l'ANSM (Agence nationale de sécurité du médicament et des produits de santé). Elle concerne la spécialité ROACTEMRA 20 mg/ml solution à diluer pour perfusion (tocilizumab) et son utilisation dans la maladie de Castleman.
ROACTEMRA (tocilizumab) a une AMM européenne
Actuellement, ROACTEMRA dispose d'une AMM (autorisation de mise sur le marché) européenne pour le traitement de certaines formes de polyarthrite rhumatoïde active et d'arthrite juvénile idiopathique systémique. La commercialisation de ce médicament est associée à un plan de gestion des risques européen. L'utilisation de ROACTEMRA est réservée à l'usage hospitalier. Sa prescription est réservée aux spécialistes en rhumatologie ou en médecine interne.
Utilisation du tocilizumab dans la maladie de Castleman
La maladie de Castleman est un syndrome lymphoprolifératif rare dont le traitement des formes disséminées n'est pas standardisé. Il s'agit d'une maladie rare.
Plusieurs études font apparaître que ROACTEMRA offre une alternative à la chimiothérapie dans les formes non plasmocytaires, non associées au virus HHV8, inflammatoires (CRP élevée) et symptomatiques de la maladie de Castleman. Le mécanisme d'action du principe actif (inhibition des récepteurs de l'interleukine-6) explique l'amélioration observée sur divers symptômes et anomalies biologiques associés à la maladie de Castleman.
Le nombre de patients potentiellement concernés est de l'ordre d'une dizaine par an.
Première RTU pour une maladie rare
Le dispositif des RTU est destiné à sécuriser l'accès à des médicaments dans des indications ou des conditions d'utilisation différentes de celles de leur AMM. La RTU est élaborée lorsque le rapport bénéfice/risque dans l'indication considérée est présumé favorable et qu'il n'existe pas d'alternative médicamenteuse appropriée.
La RTU concernant ROACTEMRA permet ainsi d'encadrer l'utilisation hors AMM de ce médicament dans le traitement de la maladie de Castleman inflammatoire (à CRP élevée) non associée au virus HHV8. A noter que cette indication est autorisée au Japon.
Un protocole de suivi définit les modalités pratiques de prescription, de délivrance, d'administration du médicament et de suivi des patients. Il précise également le rôle des différents acteurs notamment de l'ANSM, du laboratoire Roche (titulaire de l'AMM) et des prescripteurs.
En pratique
Selon le protocole de suivi établi dans le cadre de la RTU, les critères de prescription de ROACTEMRA dans la maladie de Castleman sont les suivants :
- maladie de Castleman symptomatique, multicentrique ou unicentrique non opérable ;
- âge > 2 ans ;
- indemne d'infection par HHV-8 ;
- contexte Inflammatoire : CRP > 20 mg/l en l'absence d'autre étiologie possible ;
- patient ayant arrêté la chimiothérapie et/ou la radiothérapie et/ou ayant eu leur dernière chirurgie depuis plus de 4 semaines (à l'exception d'une biopsie ganglionnaire réalisée à des fins diagnostiques) ;
- s'il s'agit d'un patient VIH positif, charge virale plasmatique < 500 copies/ml ;
- les patients présentant une tuberculose latente doivent être traités par antituberculeux avant l'instauration du traitement par ROACTEMRA.
A noter qu'après une période initiale de traitement de 3 mois, le rythme d'administration des perfusions devra être réévalué en fonction de la réponse thérapeutique. Lorsque cette dernière sera jugée satisfaisante, un espacement des perfusions toutes les 3 semaines, puis ultérieurement toutes les 4 semaines pourra être envisagé.
Pour aller plus loin
L'ANSM publie une recommandation temporaire d'utilisation (RTU) concernant la spécialité Roactemra (tocilizumab) dans la maladie de Castleman - Point d'information (ANSM, 4 avril 2014)
Fiche RTU de ROACTEMRA (ANSM, 3 avril 2014)
ROACTEMRA (tocilizumab), 20 mg/ml solution à diluer pour perfusion - Protocole de suivi (ANSM, 3 avril 2014)

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.