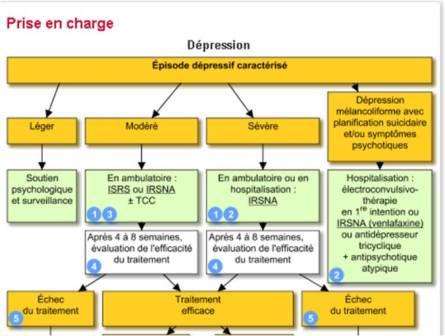
Vidal Reco "Dépression" : extrait de l'arbre décisionnel.
Le laboratoire Servier, en accord avec l'ANSM (Agence nationale de sécurité du médicament et des produits de santé) et l'EMA (Agence européenne du médicament), informe les professionnels de santé d'une nouvelle contre-indication relative à l'utilisation de VALDOXAN 25 mg comprimé pelliculé (agomélatine), destinée à minimiser le risque hépatotoxique.
Le contexte
Des cas d'atteinte hépatique parfois d'issue fatale ou ayant nécessité une transplantation, ont été rapportés depuis l'autorisation de mise sur le marché de VALDOXAN en 2009. La plupart de ces cas sont survenus au cours des premiers mois de traitement.
En octobre 2012, les professionnels de santé ont été informés :
- sur ce risque d'hépatotoxicité ;
- sur les mesures mises en place destinées à renforcer la surveillance de la fonction hépatique chez tous les patients,
- et sur la nécessité d'utiliser avec précaution cet antidépresseur chez les patients présentant des facteurs de risque d'atteinte hépatique.
La nouvelle contre-indication
Selon l'EMA, les bénéfices de VALDOXAN restent supérieurs aux risques, à condition que des mesures supplémentaires de minimisation du risque soient mises en place.
Par conséquent, VALDOXAN est désormais contre-indiqué chez les patients dont les transaminases sont supérieures à 3 fois la limite supérieure des valeurs normales.
Cette nouvelle contre-indication s'ajoute à la contre-indication chez les patients atteints d'une insuffisance hépatique, c'est-à-dire en cas de cirrhose ou de maladie hépatique évolutive.
En outre, VALDOXAN ne doit pas être prescrit chez les patients de 75 ans et plus, pour lesquels le bénéfice de ce médicament n'a pas été démontré.
Contrôler de la fonction hépatique : extrait de la Reco Vidal "Dépression"
"L'agomélatine, qui possède une action mélatoninergique et sérotoninergique, nécessite une surveillance régulière du bilan hépatique.
En effet, des cas graves d'atteinte hépatique pouvant se compliquer d'insuffisance hépatique ont été rapportés, surtout pendant les premiers mois de traitement et à la posologie de 50 mg par jour, ce qui a motivé un renforcement des mises en garde et des précautions d'emploi : bilan hépatique systématiquement contrôlé :
En effet, des cas graves d'atteinte hépatique pouvant se compliquer d'insuffisance hépatique ont été rapportés, surtout pendant les premiers mois de traitement et à la posologie de 50 mg par jour, ce qui a motivé un renforcement des mises en garde et des précautions d'emploi : bilan hépatique systématiquement contrôlé :
- à l'instauration du traitement,
- puis après 3, 6, 12 et 24 semaines (séquence à renouveler après toute nouvelle augmentation de posologie),
- et 48 heures après une augmentation des transaminases à l'occasion d'un bilan.
Le traitement sera arrêté en cas de taux de transaminases supérieur à 3 fois la normale, ou de symptômes évocateurs d'une hépatite (ANSM, octobre 2012).
L'ANSM rappelle que l'agomélatine est contre-indiquée en cas d'insuffisance hépatique préexistante (cirrhose, maladie hépatique évolutive)."
Extrait de la Reco Vidal Dépression - Traitement - Médicaments cités dans les références - Autres traitements
L'ANSM rappelle que l'agomélatine est contre-indiquée en cas d'insuffisance hépatique préexistante (cirrhose, maladie hépatique évolutive)."
Extrait de la Reco Vidal Dépression - Traitement - Médicaments cités dans les références - Autres traitements
Informer les patients sur les symptômes
Le traitement doit être immédiatement arrêté si le patient présente des symptômes ou des signes évocateurs d'une atteinte hépatique.
Ces symptômes et signes (urines foncées, selles décolorées, coloration jaune de la peau et/ou des yeux, douleur dans la partie supérieure droite de l'abdomen, apparition d'une fatigue prolongée et inexpliquée) doivent être décrits aux patients, afin de leur permettre de les repérer plus facilement et rapidement.
Ces symptômes et signes (urines foncées, selles décolorées, coloration jaune de la peau et/ou des yeux, douleur dans la partie supérieure droite de l'abdomen, apparition d'une fatigue prolongée et inexpliquée) doivent être décrits aux patients, afin de leur permettre de les repérer plus facilement et rapidement.
Pour mémoire
VALDOXAN est indiqué chez l'adulte, dans le traitement des épisodes dépressifs majeurs (c'est-à-dire caractérisés) chez l'adulte.
Sources et ressources complémentaires
Valdoxan (agomélatine) : Ajout d'une nouvelle contre-indication et rappel sur l'importance de la surveillance de la fonction hépatique - Point d'information (ANSM, 23 octobre 2013)
Lettre du laboratoire Servier aux professionnels de santé (sur le site de l'ANSM, 14 octobre 2013)
Lettre du laboratoire Servier aux professionnels de santé (sur le site de l'ANSM, 14 octobre 2013)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.