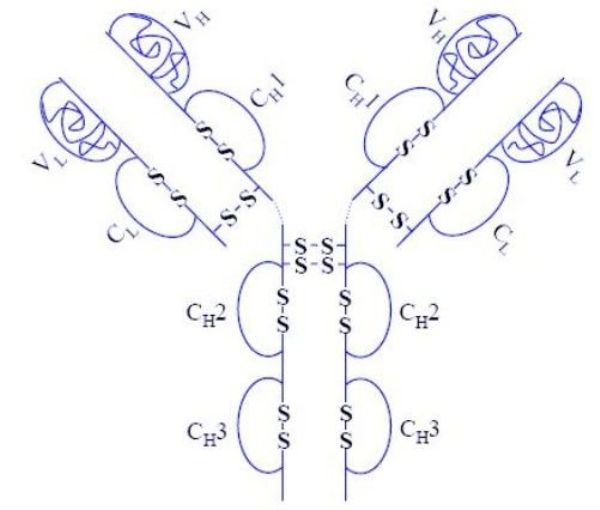
HUMIRA (adalimumab) est un immunosuppresseur sélectif, inhibiteur du TNF-alpha (source image : Wikipedia).
Le remboursement d'HUMIRA 40 mg solution injectable en seringue préremplie et en stylo prérempli est étendu au traitement de la spondylarthrite axiale sévère sans signes radiographiques de spondylarthrite ankylosante, mais avec des signes objectifs d'inflammation à l'IRM et/ou un taux élevé de CRP chez les adultes ayant eu une réponse inadéquate ou une intolérance aux anti-inflammatoires non stéroïdiens.
Pour mémoire
HUMIRA (adalimumab) est un immunosuppresseur sélectif, inhibiteur du TNF-alpha.
HUMIRA (adalimumab) est un immunosuppresseur sélectif, inhibiteur du TNF-alpha.
Le taux de remboursement d'HUMIRA est de 65 %. Ce taux ne tient pas compte des exonérations liées aux conditions particulières de prise en charge de l'assuré (ALD, invalidité, etc.).
HUMIRA est un médicament d'exception dont la prescription doit être en conformité avec la fiche d'information thérapeutique.
La prescription d'HUMIRA 40 mg en seringue préremplie et en stylo prérempli est réservée aux spécialistes en rhumatologie, en gastroentérologie, en chirurgie digestive, en dermatologie, en pédiatrie ou en médecine interne.
Sa prescription initiale est hospitalière et annuelle.
Sa prescription initiale est hospitalière et annuelle.
Outre le traitement de la spondyloarthrite axiale sévère sans signes radiographiques de spondylarthrite ankylosante, HUMIRA 40 mg solution injectable en seringue préremplie et en stylo prérempli sont indiqués dans le traitement de la spondylarthrite ankylosante sévère et active chez l'adulte ayant eu une réponse inadéquate au traitement conventionnel.
HUMIRA 40 mg solution injectable en seringue préremplie et en stylo prérempli sont également indiqués :
- en association au méthotrexate dans le traitement de la polyarthrite rhumatoïde :
- modérément à sévèrement active de l'adulte, lorsque la réponse aux traitements de fond, y compris le méthotrexate, est inadéquate ;
- sévère, active et évolutive chez les adultes non précédemment traités par le méthotrexate.
HUMIRA peut être donné en monothérapie en cas d'intolérance au méthotrexate ou lorsque la poursuite du traitement avec le méthotrexate est inadaptée.
Il a été montré qu'HUMIRA ralentit la progression des dommages structuraux articulaires mesurés par radiographie et améliore les capacités fonctionnelles lorsqu'il est administré en association au méthotrexate.
- dans le traitement du rhumatisme psoriasique actif et évolutif chez l'adulte lorsque la réponse à un traitement de fond antérieur a été inadéquate.
Il a été montré qu'HUMIRA ralentit la progression des dommages structuraux articulaires périphériques tels que mesurés par radiographie chez les patients ayant des formes polyarticulaires symétriques de la maladie, et qu'il améliore les capacités fonctionnelles.
- dans le traitement du psoriasis en plaques, modéré à sévère, chez les patients adultes qui ne répondent pas à d'autres traitements systémiques comme la ciclosporine, le méthotrexate ou la puvathérapie, ou chez lesquels ces traitements sont contre-indiqués ou mal tolérés.
- dans le traitement de la maladie de Crohn active modérée à sévère, chez les patients adultes qui n'ont pas répondu malgré un traitement approprié et bien conduit par un corticoïde et/ou un immunosuppresseur ou chez lesquels ce traitement est contre-indiqué ou mal toléré.
- dans le traitement de la rectocolite hémorragique active, modérée à sévère chez les patients adultes ayant eu une réponse inadéquate au traitement conventionnel, comprenant les corticoïdes et la 6-mercaptopurine (6-MP) ou l'azathioprine (AZA), ou chez lesquels ce traitement est contre-indiqué ou mal toléré.
Sources et ressources complémentaires
Fiche d'information thérapeutique, publiée au Journal officiel (31 mai 2013)
Pour recevoir gratuitement toute lãactualitûˋ par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.