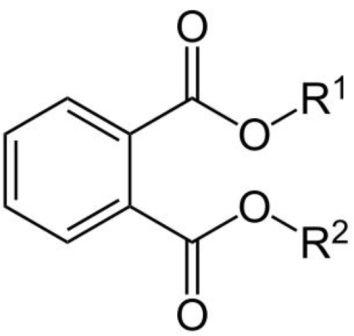
Formule topologique d’un phtalate (© Jü, Wikimédia)
Suivant le projet de recommandation de l'EMA (Agence européenne du médicament) d'encadrer l'utilisation des phtalates en tant qu'excipients dans les médicaments, l'ANSM (Agence nationale de sécurité du médicament et des produits de santé) émet des recommandations relatives à l'utilisation des médicaments contenant ces excipients au sein des populations sensibles (femmes enceintes ou allaitantes, et enfants).
Les phtalates en question
Les phtalates entrent dans la composition de dispositifs en plastique, dont les dispositifs médicaux, auxquels ils confèrent leur propriété flexible.
Ils sont aussi utilisés comme excipients dans les médicaments, principalement comme plastifiant pour enrobage (enrobage gastro-résistant des comprimés ou enrobage des formes à libération prolongée).
Plus précisément, 5 phtalates sont utilisés dans les spécialités pharmaceutiques :
- le phtalate de dybutile (DBP) ;
- le phtalate de diéthyle (DEP) ;
- l'acétate phtalate de polyvinyle (PVAP) ;
- le phtalate d'hypromellose (HPMCP) ;
- l'acétate phtalate de cellulose (CAP).
Nocivité des phtalates
Des effets endocriniens potentiels ont été attribués à ces composés et des études sont en cours afin de déterminer les risques pour l'homme.
Certains phtalates sont classés comme substances reprotoxiques pour l'espèce humaine (règlement européen 1272/2008 du 16/12/08 relatif à la classification, à l'étiquetage et à l'emballage des substances et des mélanges).
Certains phtalates sont classés comme substances reprotoxiques pour l'espèce humaine (règlement européen 1272/2008 du 16/12/08 relatif à la classification, à l'étiquetage et à l'emballage des substances et des mélanges).
Mais, "Les données cliniques disponibles concernant les effets potentiels des phtalates chez l'homme ne permettent pas d'exclure un risque, en particulier pour les populations sensibles comme les enfants exposés in utero, les nouveau-nés exposés via l'allaitement et les enfants exposés directement", précise l'ANSM.
Selon les données disponibles, seuls le DBP, le DEP et le PVAP seraient toxiques.
Cinq spécialités concernées
Selon l'ANSM, ces phtalates entrent dans la composition d'environ 150 spécialités pharmaceutiques.
Parmi ces spécialités, cinq présentent des quantités de phtalates supérieures à celles recommandées par l'EMA :
- ACADIONE 250 mg comprimé dragéifié (tiopronine) ;
- ATRICAN 250 mg capsule molle gastrorésistante (ténonitrozole), dont la commercialisation est arrêtée depuis 2012 ;
- PROKINYL 15 mg gélule à libération prolongée (métoclopramide) ;
- ROWASA 250 mg et 500 mg comprimé enrobé gastrorésistant (mésalazine).
L'ANSM a demandé aux laboratoires titulaires des AMM (autorisations de mise sur le marché) de ces 5 spécialités, de les reformuler dans un délai de 18 mois afin de disposer de formes pharmaceutiques dépourvues de cet excipient.
Le RCP (résumé des caractéristiques du produit) et la notice de ces spécialités sont en cours de modification pour informer les professionnels de santé et les patients traités de la présence de phtalates parmi les excipients et permettre ainsi de limiter l'exposition des personnes les plus sensibles aux effets potentiels des phtalates (femmes enceintes et allaitantes, enfants) durant cette période transitoire.
En pratique
En attendant ces modifications, l'utilisation de ces spécialités doit être limitée dans la mesure du possible pour les populations sensibles :
- la femme enceinte, afin de limiter l'exposition in utero aux phtalates ;
- la femme allaitante, afin de limiter l'exposition de l'enfant via l'allaitement ;
- les enfants, afin de limiter l'exposition directe.
L'Agence demande aux professionnels de santé, pour les populations à risque (femmes enceintes et allaitantes, enfants) :
- de favoriser quand cela est possible les alternatives thérapeutiques dépourvues de phtalates (autres spécialités contenant le même principe actif et ne comportant pas de phtalates parmi ses excipients, ou autres spécialités contenant un principe actif différent mais ayant la même indication thérapeutique) ;
- de limiter, en l'absence d'alternative, le traitement par les spécialités concernées à la durée la plus courte possible et à la dose efficace minimale.
Sources et ressources complémentaires
L'ANSM impose des précautions d'emploi pour 5 spécialités contenant des phtalates en quantité supérieure au seuil recommandé par l'Agence Européenne - Point d'information (ANSM, 23 juillet 2013)
Compte-rendu de la séance n°1 du 25 avril 2013 de la Commission prévention des risques liés à l'utilisation des catégories de produits de santé (ANSM, 23 juillet 2013)
Phtalates et médicaments - Questions/ Réponses (ANSM, 23 juillet 2013)
Phtalates et médicaments - Questions/ Réponses (ANSM, 23 juillet 2013)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire.jpg)

.jpg)




Commentaires
Cliquez ici pour revenir à l'accueil.